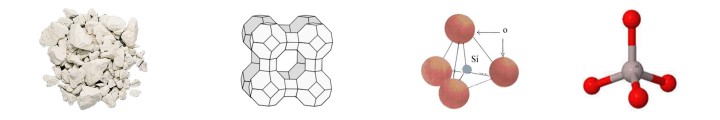
모데나이트란?
1. 모데나이트의 정의
- 13차원 구조를 갖는 알루미노 규산염(aluminosilicate)의 총칭을 일컫는다.
- 2결정성 다공성 물질이며 정사면체의 기본 단위로 나노 크기의 세공을 가지고 있다.
- 3결정 내부에 존재하는 특이한 세공 구조 때문에 산업적으로 유용한 각종 물리화학적 특성을 갖는 천연 및 합성 광물질을 일컫는다.
| 다공성 물질 | 결정성 | 제올라이트*, 점토 등 | *제올라이트 광물군: 고다나이트, 그멜리나이트, 메솔라이트, 브로스테라이트, 모데나이트(Mordenite), 방비석, 스콜레사이트 등 50종류 이상 |
| 무정형 | 실리카, 알루미나, 활성탄 등 | ||
2. 모데나이트의 특성
1) 흡착 성질
a) 분자체(Molecular Sieve)
- 13차원 구조, 규칙적이고 세공모양과 크기가 일정 분자 크기에 따라 통과 가능성이 결정됨 -> 분자체
- 2소성하면(섭씨 ~500도) 탈수, 골격 구조(세공)유지 - 흡착 공간
- 3가역적인 탈착, 흡착 가능 - 흡수(분리)제로 활용
-
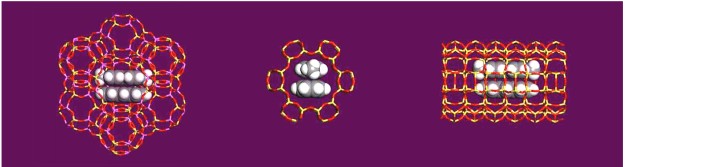
[J. Phys. Chem. 1993, 97, 6492-6499]
b) 친수성과 소수성
| 물의 흡착등온선 (25 ->) | 물과 사이클로헥산의 흡착등온선 |
| * Si / Al = 1 근처의 모데나이트(제올라이트)는 친수성이 강함 * Si / Al = 20 인 모데나이트(제올라이트)는 표면이 소수성임 |
2) 양이온 교환 능력
- 1골격중심원자가 Si, Al로 이루어진 모데나이트는 전기적 중성을 띄지 않고 음전하를 띠기 때문에 양전하가 붙어야 전기적 중성을 이룰 수 있다. (Si = +4, Al = +3)
- 2Na+ 이온이 있는 모데나이트가 채워진 관에 경수를 통과시키면 Na+ 이온이 Ca2+, Mg2+ 로 바뀐다. (경수의 연수화)
- 3모데나이트는 광물질 중에서 가장 뛰어난 양이온 교환 능력을 지님
3) 산.염기성
- 1알루미늄이 포함된 제올라이트는 산, 염기성을 가짐 (양전하 부족 ⇒ 골격이 음전하를 띄기 때문)
① 전기적 중성을 만들어주기 위해 양전하 필요
② 제올라이트 내 양전하와 음전하를 띄는 부분이 생김
③ 산, 염기성이 생김 - 2전자 밀도가 낮은 산점과 전자 밀도가 높은 염기점이 생기고, 이러한 특성을 조절하여 촉매나 흡착제로 사용
4) 촉매
- 1넓은 표면적 (세공내부 ~ 500m2/g)
- 2조절가능한 산성도 (제올라이트의 종류, 양이온, Si / Al 몰비 등)
- 3금속이나 산화물을 고정하는 안정된 결정성 구조
- 4규칙적인 세공으로 형상선택적 촉매 작용
3. 천연모데나이트의 일반적 성질
1) 방사성 양이온 흡착 제거
- 11가 세슘(Ce+, 134.337)이온은 모데나이트 세공내부에서 K+, Na+ 양이온과 교환반응
- 22가 스트론튬(Sr++, 핵종)은 mordenite Ca++, Mg++ 2가 양이온과 교환 반응. 모데나이트 세공내부는 영구전하 성능을 가지고 있어 흡착한 양이온을 불용화 시킨다.
2) 산.염기성
- 1Mordenite내 양전하, 음전하를 띄는 부분이 생김 그러므로 산,염기성이 생긴다. 즉, 전자밀도가 낮은 산점(Lewis acid side)과 전자밀도가 높은 염기점(Bronsted acid side)이 생김
3) 이온교환수지화와 같은 기능, 활성탄과 같은 강력한 흡착력
4) 일반적 이온교환 선택성
- 1Cs+>Rb+>K+>NH4+>Ba+>Sr+>Na+>Ca++>Fe++>Al3+>Li+
이 들의 흡착고정화는 극단적인(강산성, 강알칼리성)환경 변화가 없다면 방출되는 일이 없다.
| 구 분 | 성 능 | 비 고 |
| pH | 6 ~ 7 | |
| 비중 면적 | 600m2/g | |
| 영구하전 | CaO, MgO, K2O, Na2O | 주1) |
| 양이온 치환력(CEC) | ~170meq/100g | 주2) |
| 탈취성능 | 활성탄의 10배 | |
| Si / Al 몰비 | 4.4 ~ 5.5 | 주3) |
| 표면적 | ~500m2/g | |
| 겉보기 비중 | 약 1.3 ~ 4 | |
| 비중 | 2 ~ 2.7 | |
| 세공 크기 | 1nm 이하 | 1nm = 1/100만mm |
| 1) 모데나이트 세공 내부는 영구전하 성능을 갖고 있어 흡착한 양이온을 불용화 시킨다. 2) 순도 100%의 경우 이론치 223meq/100g 3) High silica군, 수 환경에 안전함 - 촉매나 특수 흡착제 이용에 중요한 요인으로 작용 |
4. 모데나이트의 응용
1) 흡착 및 분자체 특성 응용
- 1중금속 흡착: 천연 모데나이트를 액상화 한 액체 모데나이트는 몸속의 중금속, 노폐물, 독소 등을 흡착 제거 하여 체외로 함께 배출시킨다. (가격이 비쌈)
- 2탈취제: 모데나이트의 세공이 흡착 제거 하여 탈취 효과를 낸다. 또한, 열에 강하기 때문에 높은 온도에서도 연소가 되지 않아 열처리를 통해 쉽게 흡착한 것을 탈착하고 다시 흡착 할 수 있다.
- 3흡습제: 탈취제와 비슷한 원리이다. 300~400도(섭씨)에서 가열한 탈수 된 모데나이트를 대기중에 방치하면 수분을 흡수하므로 흡습제로 사용할 수 있다.
탈취제로 많이 쓰이는 모데나이트 구조: 세공의 비어있는 부분이 전체의 40% 정도 되며, 세공 내 표면적이 넓어서 흡착 용량이 크다. - 4토양 개량제: 모데나이트는 세공 부피에 해당하는 물을 항상 가지고 있기 때문에, 장마철에 배수가 잘 되어 식물의 뿌리가 썩지 않게 하고, 가뭄에는 모데나이트 내의 수분이 땅이 갈라지는 것을 방지해 준다.
- 5건축자재: 모데나이트는 열전도도가 낮은 공기가 채워진 세공이 많아 단열효과가 우수하고, 습도 조절 기능이 있기 때문에, 건축용 벽돌로도 사용되며 기능성 페인트의 첨가제로 쓰이기도 한다.
2) 양이온 교환 특성 응용
- 1합성세제(4A형 Zeolite): 초창기 합성세제엔 Ca2+, Mg2+ 를 제거하기 위해 인산염을 사용하였으나 인산염이 호수의 부영화의 원인이 되었는데, 제올라이트는 무기물이기 때문에 부영양화 같은 부작용 없이 센물을 단물로 바꾸어 줄 수 있다.
- 2향균제: 일반적으로 4A형 Zeolite의 Na를 향균 효과가 높은 Ag, Cu, Zn 과 같은 금속이온으로 양이온 교환을 통해 제조한다. 제올라이트 같은 이온교환형 향균제는 점착, 착염식 향균제 보다 훨씬 구조적으로 안정적이고 향균력이 지속적으로 나타나게 된다. 대표적인 제올라이트계 향균제로는 [Ag-Zn-Zeolite A]가 있다. (Na를 Ag와 Zn으로 양이온 교환하여 만들었다는 의미)
- 3흡습제: 탈취제와 비슷한 원리이다. 300~400도(섭씨)에서 가열한 탈수 된 모데나이트를 대기중에 방치하면 수분을 흡수하므로 흡습제로 사용할 수 있다.
탈취제로 많이 쓰이는 모데나이트 구조: 세공의 비어있는 부분이 전체의 40% 정도 되며, 세공 내 표면적이 넓어서 흡착 용량이 크다. - 4토양 개량제: 모데나이트는 세공 부피에 해당하는 물을 항상 가지고 있기 때문에, 장마철에 배수가 잘 되어 식물의 뿌리가 썩지 않게 하고, 가뭄에는 모데나이트 내의 수분이 땅이 갈라지는 것을 방지해 준다.
- 5건축자재: 모데나이트는 열전도도가 낮은 공기가 채워진 세공이 많아 단열효과가 우수하고, 습도 조절 기능이 있기 때문에, 건축용 벽돌로도 사용되며 기능성 페인트의 첨가제로 쓰이기도 한다.
| 제올라이트의 대표적인 구조도. Y형과 X형은 가운데 세공의 크기가 7.4A, 4A형은 4.2A이다. 4A는 이온교환을 통한 응용(향균제, 합성세제용)에 적합하고, Y(X)는 큰 세공을 이용한 흡착 응용(탈취, 소취)에 적합한 구조이다. Y형과 X형은 Si / Al 비율은 다르지만 골격 구조는 같은 형태이다. |
5. 특허 및 시험 성적서
-
특허증
-
CEC / 항균시험
-
탈취시험(암모니아)
-
탈취시험(암모니아/황화수소)
-
탈취시험(아세트알데하이드)
-
성분원소 분석시험
-
성분시험(게르마늄, 바나듐)
-
성분시험(게르마늄, 바나듐, 셀레늄)
-
항균 및 수질시험
-
환경부 고시(제2008-69호)